食紅を使ったタンパク質の定量法(Bradford法の様に)〜自宅でできる簡単な研究(FR-2.1)
このテーマのきっかけである「蕎麦粉の成分分布の違いを科学的に調べられないか」について、試料の成分を呈色反応でデジタル画像から数値化する方法は、デンプンやタンパク質を測定する実験の構想、食紅をモデルにした呈色反応のデジタル画像取得法、ImageJを用いた呈色反応モデルの画像解析法でほぼ確立しました。
ここでは、食紅を使ってタンパク質の量を数値化(定量)出来るかどうかを検討してみました。
何かの役には立たないし、人から見たらどうでも良いことで自己満足の世界でありますが、デンプンやタンパク質を測定する実験の構想で述べた構想をもとに個人研究として取り組んでいます。
目次
1. 食紅とタンパク質の反応
2. クエン酸と食酢の濃度検討
3. 酸によるローズベンガルの退色は可逆性
4. タンパク質の定量
5. ローズベンガルの反応イメージ
6. 課題
1. 食紅とタンパク質の反応
タンパク質を呈色反応で定量化するBradford法をモデルとしました。Bradford法は、個人では試薬の入手と廃液の処理が困難で不可能と判断し、食紅で代用出来ないか検討しました。
酸性溶液中で、青色色素の Coomassie Brilliant Blue G-250 がタンパク質と結合することで、最大吸収波長が 465nmから595nm にシフトすることを利用して タンパク質を定量する方法。参照
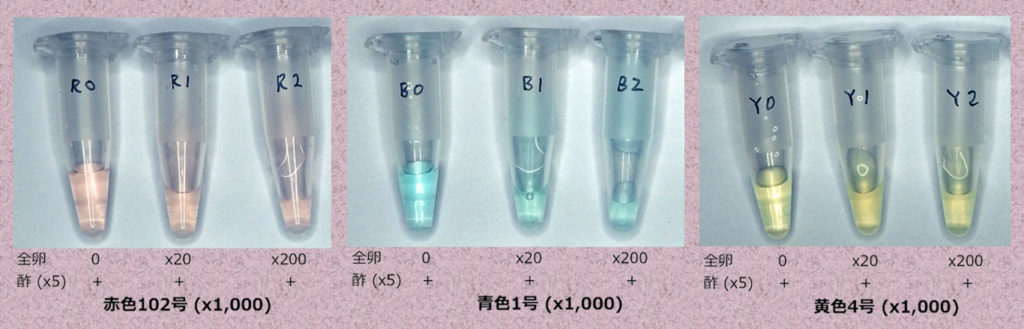
食紅の赤色102号、青色1号、黄色4号それぞれにタンパク質として、全卵を水で薄め10倍の希釈系列を反応させました。さらに色が変化することを期待し食酢を加えてみましたが、変化はありませんでした(下の写真)。
次に、食紅の赤色105号(ローズベンガル, Rose Bengal)を同様に試してみたところ、ローズベンガルは食酢を加えると色が消え、タンパク質が存在すると赤色のままで、10倍の希釈系列で色の濃さが変わりますした(下の写真)。
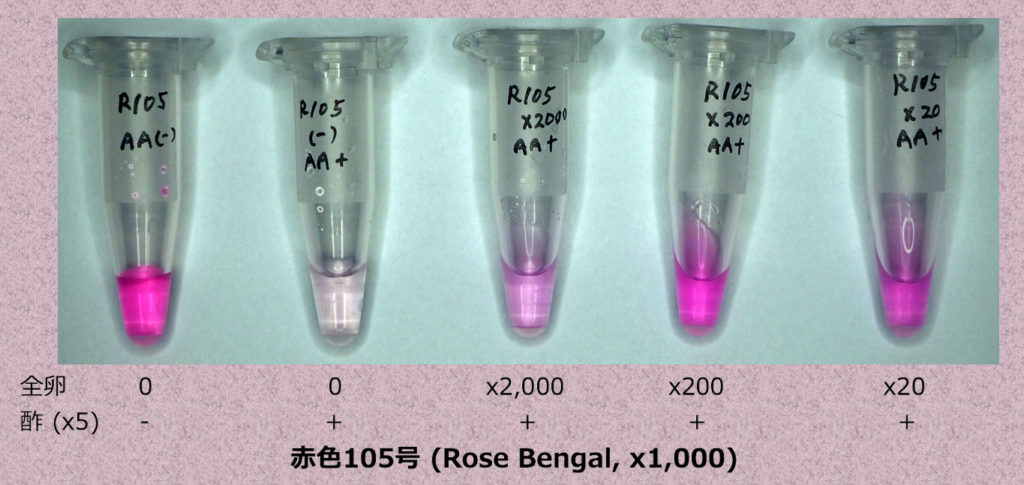
食品や生体試料などを赤色に着色するために用いる着色料で、赤色105号として食品添加物の指定を受けている。
眼科では、ローズベンガル液を点眼して、角結膜の障害を調べる(涙液の分泌低下により角結膜が障害されると染色される)検査に使われています。
歯科では、歯垢の主成分が微生物及びその産生物などからなる有機質であることを利用して、ローズベンガルで染色して歯垢の有無の検出に使われています。

2.クエン酸と食酢の濃度検討
ローズベンガルに食酢を加えると退色することから、これは酸性による退色と考えました。食酢は、酢酸の他アミノ酸などが含まれているため、クエン酸を食酢の代わりに使用することにしました(注:以下、濃度は最終濃度を示します)。
ローズベンガルは、簡単な検討で濃度が20ug/mL付近が退色に良いことが分かっています(下の写真)。

ローズベンガルの濃度を20ug/mLに固定し、クエン酸の濃度を10mMから2倍の希釈系列を作製して色の変化を調べました(下の写真)。

また、食酢についても希釈16倍から2倍の希釈系列を作製し色の変化を作製しました(下の写真)。
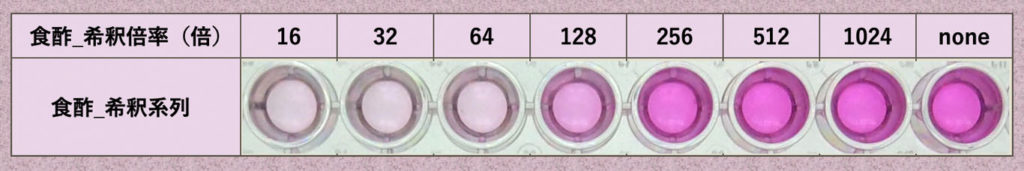
これらの結果を、ImageJを用いた呈色反応モデルの画像解析法で示した解析法を行いグラフにしました。吸光度に相当する補色のGチャンネル強度を縦軸にしています(下の図の左はクエン酸で、右が食酢)。
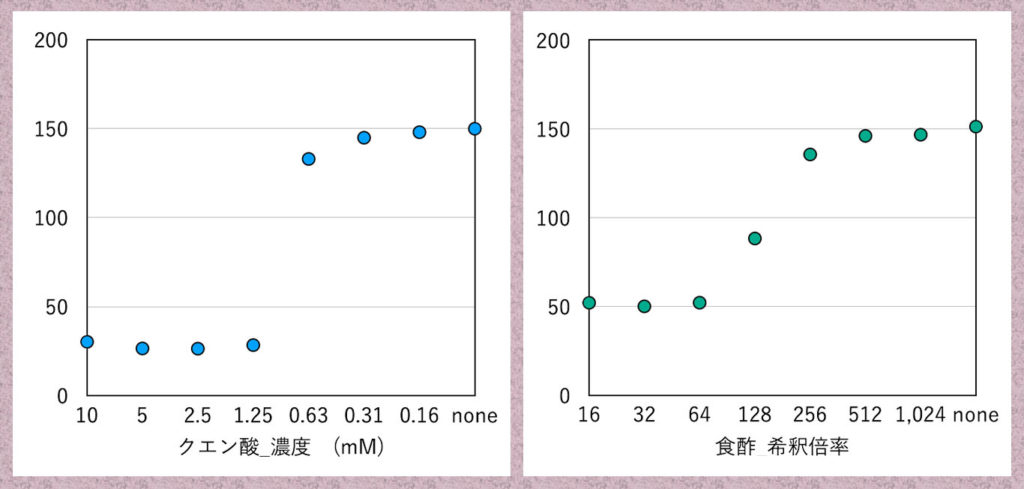
クエン酸は、0.63mMから1.25mMの付近で色の変化が認められます。食酢は、64倍から256倍付近でなだらかに変化が見られ、濃度を濃くしても赤色が残る結果となりました。
この結果から解析にはクエン酸を使用し、濃度は安全を見越して濃度5mMで行うことに決定しました。
3.酸によるローズベンガルの退色は可逆性
クエン酸や食酢によって退色したローズベンガルは、アルカリを加えることで(中性にする)発色が戻るかどうかを調べました。
アルカリ溶液は、重曹を使用しました。重曹を濃度250mMから2倍の希釈系列を作製し、濃度5mMのクエン酸と24倍希釈の食酢で退色したローズベンガル溶液に加えました(下の写真)。
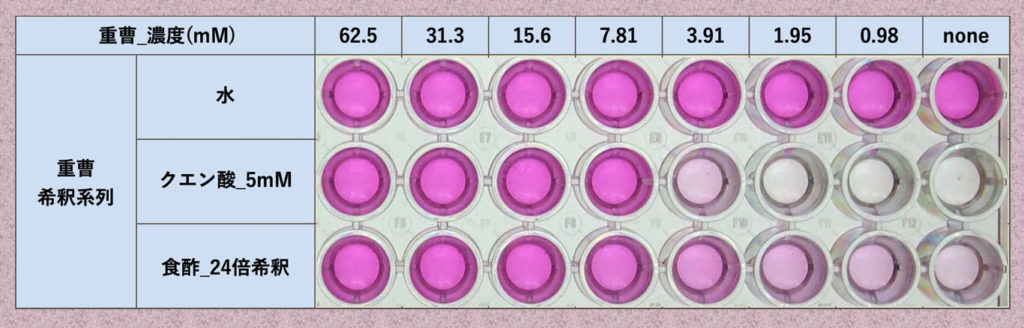
重曹により中性すると酸によって退色していたローズベンガルの発色が回復しました。またアルカリ性では、発色に変化はありませんでした。下にGチャンネルの結果をグラフにしました。棒グラフは重曹のみで、散布図は左がクエン酸と重曹、右が食酢と重曹です。
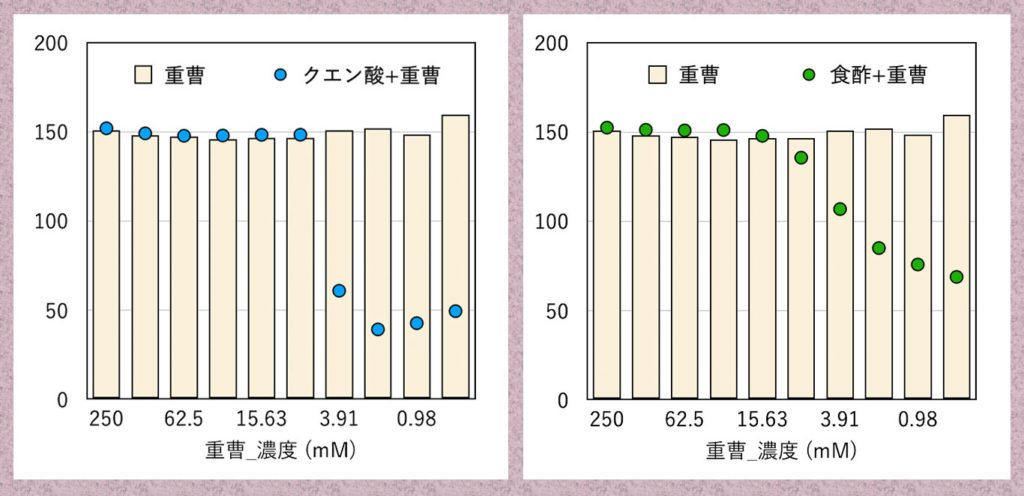
4.タンパク質の定量
タンパク質は、全卵より成分が均質なゼラチンを使用することにしました。
ゼラチンを濃度100ug/mLから2倍希釈系列を作製し、濃度20ug/mLのローズベンガルを加えました。最後に、濃度5mMのクエン酸を加え反応させました(下の写真)。
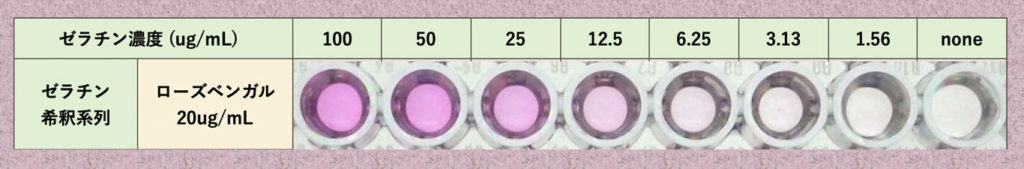
ゼラチンの濃度によりローズベンガルの色が変化しました。
この結果をグラフにしました(下の図、横軸は、logスケールです)。
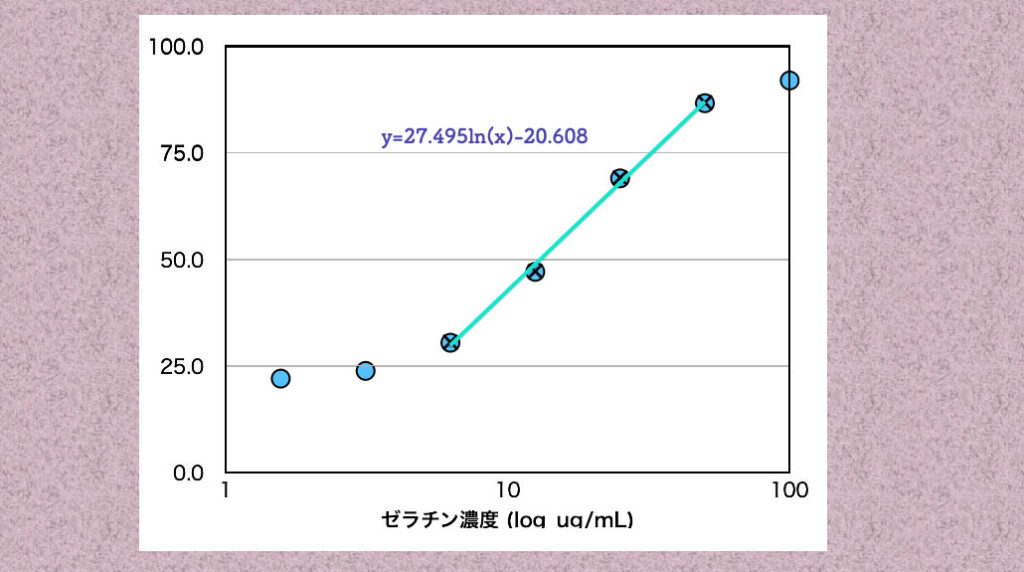
ゼラチンの濃度が6.25ug/mLから50ug/mLの間で直線性が得られました。
ローズベンガルがタンパク質以外の試料に反応するか調べました。食品に含まれる主成分の1つである炭水化物(デンプン)には、片栗粉を使用しました。片栗粉は、濃度250ug/mLから2倍の希釈系列を作製し、ゼラチンと同じ条件(濃度20ug/mLのローズベンガル、濃度5mMのクエン酸)で反応させました。また、片栗粉水溶液の希釈系列を確認するため、デンプンに反応するポピドンヨード液を濃度40倍で(クエン酸は入っていません)使用しました(下の写真)。

ローズベンガルは、デンプンとは反応しないことがわかりました。今のところ、タンパク質に特異的に反応し、タンパク質定量が出来そうです。
5.ローズベンガルの反応イメージ
ローズベンガル、タンパク質と酸の関係は、下の図をイメージしております。
ローズベンガル(RB)は、タンパク質と吸着して酸(H+)からの攻撃を受けず赤色に発色します。一方、フリーのローズベンガルは、酸の攻撃を受け発色せず透明になります。この現象から、タンパク質の量がローズベンガルの発色との相関関係が成立し、タンパク質量を計測することが可能となったと考えています。
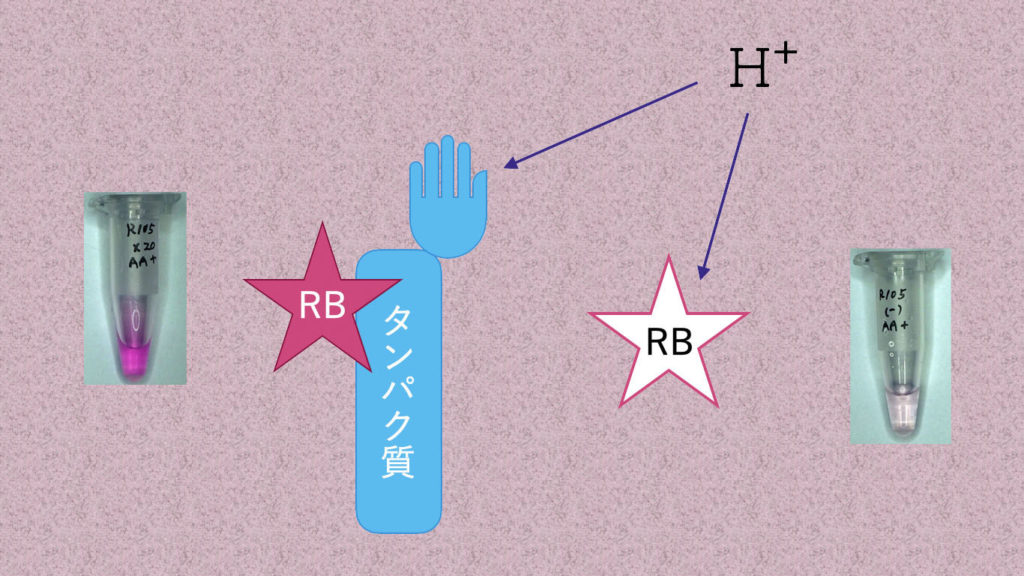
しかし、ローズベンガルとクエン酸を反応させ後、ゼラチンを加えても発色しませんでした。そのまま放置し、翌日観察すると少しだけ発色が認められたことから、もう少し複雑なイメージ図になると思います。
6.課題
この実験は、もう少し詳しく調べてみようと思います。課題として、
・反応の順番による発色の違い
・タンパク質の種類による反応(発色)の違い
・タンパク質濃度の濃いところと薄いところでの検量線について
・タンパク質のpIによるpHの影響
・特異性(他の成分、例えばアミノ酸など)について
などです。個人で購入できる試料・試薬・器具は限られますが出来る範囲で調べてみようと思います。





ディスカッション
コメント一覧
まだ、コメントがありません