紫キャベツと巨峰を使った酸性とアルカリ性による色の変化について〜自宅でできる簡単な研究(FR-3.2)
身近な食品の中には、アントシアニンが多く含まれるものがあます。その紫色の色素を抽出した溶液に酸性やアルカリ性のものを加えると色が変化します。代表的な食品として紫キャベツがありますが、季節によって入手困難な時期があります。そこで、長期保存の方法として乾燥した紫キャベツを作り、それを使い実験してみました。また、巨峰ぶどうの皮についても同様に検討してみました。
何かの役には立たないし、人から見たらどうでも良いことで自己満足の世界でありますが、個人研究に取り組んでいます。
目次
1. 紫キャベツ
1-1. 乾燥紫キャベツの作製と紫色素(アントシアニン)の抽出
1-2. 抽出液の酸・アルカリによる色の変化
2 ぶどう(巨峰)の皮
2-1. 乾燥巨峰ぶどうの皮の作製と紫色素(アントシアニン)の抽出
2-2. 抽出液の酸・アルカリによる色の変化
2-3. 抽出方法を変えて検討
3. クエン酸緩衝液の作り方
1. 紫キャベツ
1-1. 乾燥紫キャベツの作製と紫色素(アントシアニン)の抽出
紫キャベツは、スーパーで1/4カットの物を購入しました(下の写真左)。食事に使う分の残りをざるで天日干ししました(下の写真右)。

天日干しした紫キャベツは、冷蔵庫で保存しています。下の写真(A)の様に茶色く紫色は目立ちません。抽出方法は、ナスニンの時(ナスの色素(ナスニン)の酸性とアルカリ性による色の変化について)と同様に乾燥紫キャベツ1gに水10mLを加えビニール袋の中で揉み、アントシアニンを含む溶液を抽出しました(下の写真(B)、(C))。濾紙などで濾過はしませんでした。

1-2. 抽出液の酸・アルカリによる色の変化
アントシアニンは、酸性の時には赤色に、アルカリ性の時には青色になる性質が知られています。紫キャベツから抽出したアントシアニンが含まれる溶液で、酸・アルカリによる色の変化を調べてみました。
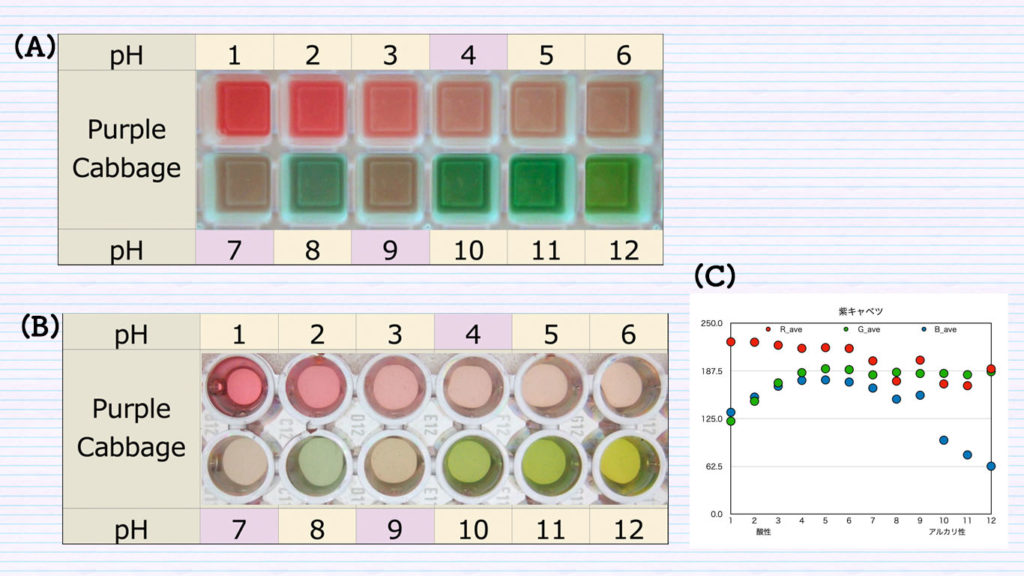
下の写真がその結果です。(A)は製氷皿で1mLの酸性・アルカリ性の各溶液に100uLの紫キャベツ救出液を加え反応させた結果で、(B)はその溶液を96穴のマイクロプレートに200uL入れて観察した結果です。
それぞれの酸性・アルカリ性溶液は、大まかですが番号がpH値を表しています。(C)は、それぞれの透過光のR,G,B-チャンネルの値をImageJにて解析し、グラフにしました。解析方法の詳細は、「ImageJを用いた呈色反応モデルの画像解析法」に掲載しています(吸収光の解析方法)。
酸性では、青と緑の透過光の割合が低く赤色が強くなり、アルカリ性では、青の透過光が低く黄緑になることがグラフから分かりました。
使用した酸性・アルカリ性溶液は、
1. サンポール x20 (5%):一般情報によるpH
2. 0.1M クエン酸:一般情報によるpH
3. クエン酸-クエン酸ナトリウム (pH 3.0):pH試験紙によるpH
4. Standard pH 4.00
5. クエン酸-クエン酸ナトリウム (pH 5.5):pH試験紙によるpH
6. クエン酸-クエン酸ナトリウム (pH 6.0):pH試験紙によるpH
7. Standard pH 6.86
8. 0.1M 重曹:一般情報によるpH
9. Standard pH 9.18
10. 0.1M セスキ炭酸ナトリウム:一般情報によるpH
11. 0.2% アンモニア水:一般情報によるpH
12. 1% アンモニア水:一般情報によるpH
番号の 4, 7, 9 は、下の写真 (A) のpH 4, 7, 9 標準液を使用しました。
番号の 1, 2, 8, 10, 11, 12 は、一般的に言われている溶液のpHの値をそのまま使いました。
番号の 3, 5, 6 は、クエン酸バッファー調整法を参考に、下の写真 (B) のpH試験紙を使用して調整しました。
また、番号8と9の色が逆転している様な結果になりましたので、pH試験紙(下の写真(B))で調べてみました。下の写真(C)がその結果です。左端の「Sample」が番号8の0.1M 重曹溶液で、右隣のpH9.18標準液と差が認められませんでした。0.1M重曹液はpH8.2位と言われていますが、番号8の重曹液はpH9より高い可能性が示されました。

アントシアニンを抽出する時、紫キャベツの量を多くすると中性付近の色の違いが鮮明になるかも知れません。
2 ぶどう(巨峰)の皮
2-1 乾燥巨峰ぶどうの皮の作製と紫色素(アントシアニン)の抽出
次に、ぶどう(巨峰)の皮も紫キャベツと同じ様にアントシアニンを抽出しました(下の写真(A)から(D))。ぶどうの皮2gに7mLの水で抽出をしています。

2-2. 抽出液の酸・アルカリによる色の変化
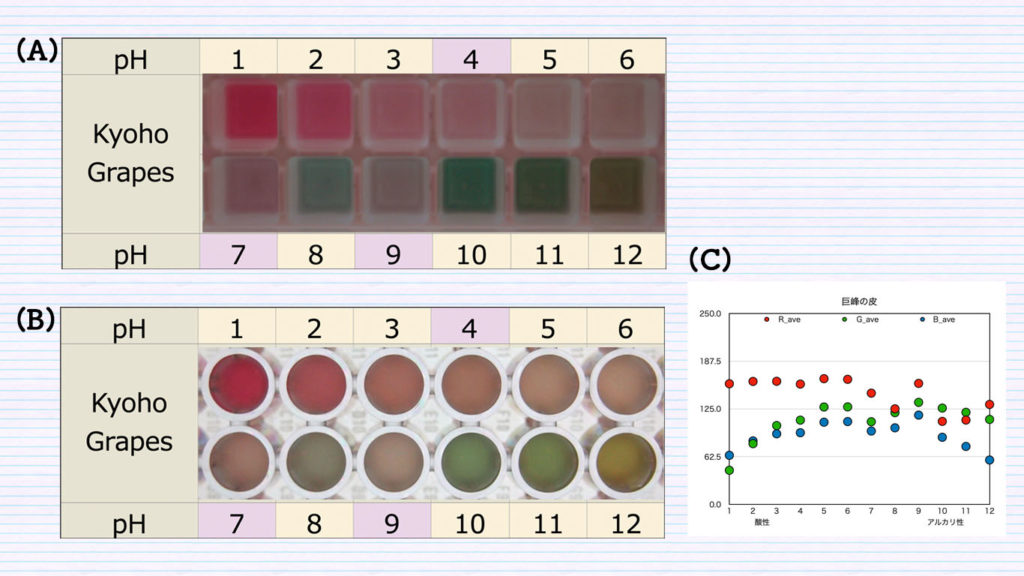
結果は、下の写真の様になりました((A)が製氷皿、(B)がマイクロプレートで(D)がグラフ)。抽出する時、ぶどうの実の部分も多く抽出されたためか溶液が濁った状態でした。
2-3. 抽出方法を変えて検討
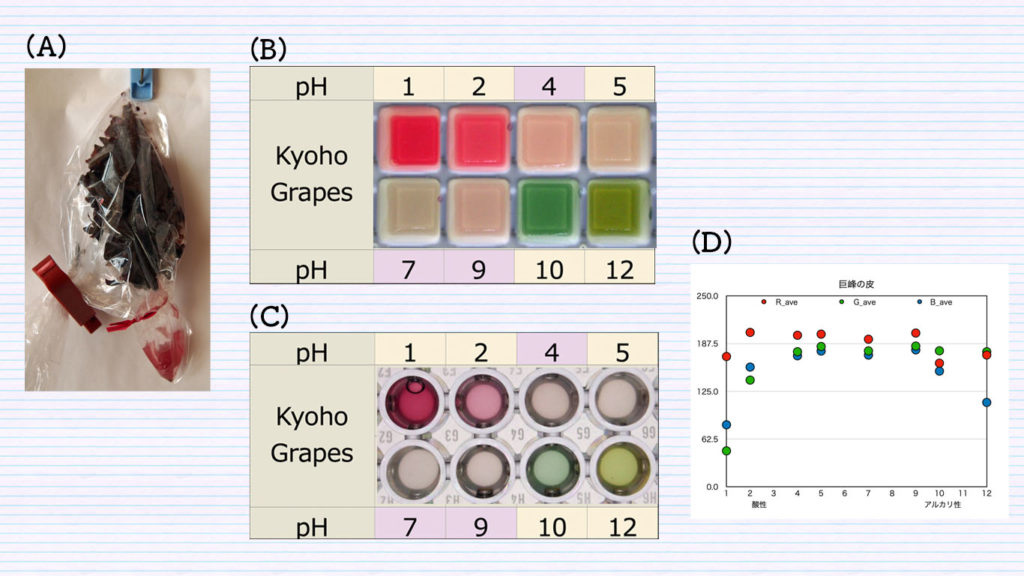
ぶどうの皮7g(ぶどう一房分です)に7mLの水をビニール袋に入れ、揉まずに少しの間静置してビニールにねじりっこで皮が下に行かない様に途中で止めて抽出液をビニール袋の下に集めた後、端をハサミ切って回収しました(下の写真(A))。結果は、下の写真(B)が製氷皿、(C)が96穴マイクロプレート、(D)がグラフです。
溶液の濁りは少なくなり、良好な結果を得ることが出来ましたが、巨峰は高価で効率が良くないと思います。
3. クエン酸緩衝液の作り方
酸性溶液のpH3, 5, 6付近の溶液は、クエン酸を希釈して作る方法もありますが緩衝液の方が安定性があるのでクエン酸緩衝液を作ることにしました。
しかし、クエン酸3ナトリウムは、個人で購入しようとすると入手困難でした。100円均一でも入手可能なクエン酸と重曹(下の写真(A))を使ってクエン酸3ナトリウムを作ることにしました。
反応式は、
C6H8O7 +3NaHCO3 → Na3C6H5O7 + 3CO2 + 3H2O
となります。クエン酸と重曹を反応させると、クエン酸3ナトリウムと炭酸と水になります。
クエン酸は分子量が192.124で、重曹は分子量が84.007ですので、0.1M クエン酸3ナトリウム(正確には0.1Mにはなりませんが)を作るには、クエン酸 1.92g と 重曹 2.521g (下の写真(B))を100mLの水に溶かします。
溶かした直後から炭酸ガスが発生しますので(下の写真(C))泡の発生が収まるまで反応させます。その時点での溶液は、BTB試薬で反応させると酸性を示していました。
その後、電子レンジで500W,1分加熱すると再び泡が発生します。撹拌して泡の発生が収まったら室温に冷やします。それをBTB試薬で反応させるとアルカリ性を示していました(下の写真(E))。
この溶液を0.1M クエン酸3ナトリウムとして、0.1M クエン酸と反応させて「クエン酸バッファー調整法」を参考にクエン酸緩衝液を作りました。
クエン酸溶液は、pH試験紙で確認して大まかなではありますがpH3, 5, 6の溶液を作製し、上記の実験に使用しました。

クエン酸は無水と表記されていましたが、重曹は水和物の表記がありませんでした。今回は無水と仮定して使用しております。個人で購入できる試薬には限界があるので重曹の純度などから番号8のような結果が得られたのかも知れません。
お菓子作りに使われる紫芋パウダーを購入して実験した結果を「紫芋パウダーを使って酸性・アルカリ性の色変化を調べる」に掲載しました。







ディスカッション
コメント一覧
まだ、コメントがありません